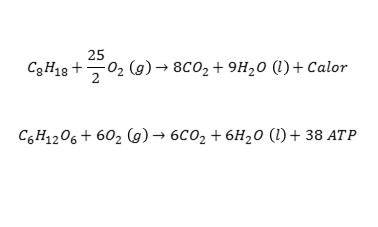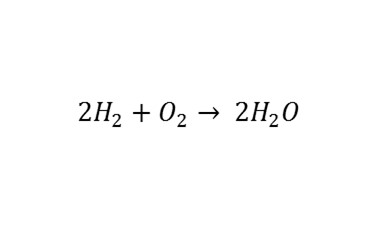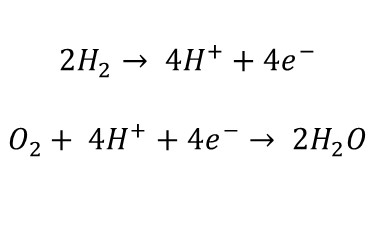Energía. Todos entendemos, en principio, qué es. Pero seguramente, si nos pidieran definirla caeríamos en un lodazal de imprecisiones, en un mar de banalidades que no acabarían de aclarar el concepto. En situaciones como esta conviene acudir a los amigos físicos, que con su frío pragmatismo van al núcleo de la cuestión, sin rodeos, sin prolegómenos. La física clásica define la energía como la capacidad para realizar un trabajo. Y aunque en esta definición “trabajo” tiene un sentido muy concreto (alterar el estado de movimiento de un cuerpo), me gusta porque también funciona con el resto de acepciones. Energía es lo que nos mueve, lo que hace que actuemos, el poder, la virtud para obrar.
Una frase muy manida que nos viene a la cabeza al hablar de energía es esa de que: “La energía ni se crea ni se destruye, sólo se transforma”, ley de conservación de la energía o primer principio de la termodinámica, que viene a decir que energía hay la que hay, y punto; que no podemos generar más. Nos tenemos que apañar. Por suerte, parece que hay suficiente, pero, ¿de dónde sale?
En una escala de tiempo cósmica habría que decir que la energía (como en realidad todo lo que conforma el Universo) proviene del Big Bang donde estaba cohesionando toda esa materia densa que reventó. A partir de ese momento se empezaron a combinar las partículas subatómicas (protones, neutrones y electrones) para formar los átomos que conocemos. En esas combinaciones se invirtió y se liberó energía. Tal como sigue ocurriendo hoy. Si reducimos un poco la escala espacio-temporal y nos centramos en la Tierra, gran parte de la energía proviene del Sol, donde la reacción de fusión de dos átomos de hidrógeno para formar uno de helio libera energía que llega a nuestro planeta en forma de radiación. Hay otras fuentes de energía, como la que emana en forma de calor del núcleo de la tierra, y que se aprovecha en las explotaciones geotérmicas, pero vamos a centrarnos en la solar, que es la que más aprovechamos los seres vivos.
La energía que llegaba del Sol generó las condiciones en las que se desarrolló la vida tal como la conocemos. Los organismos vivos desarrollaron a su vez estrategias de transformación y acumulación de energía para su desarrollo, que básicamente consisten (siguen vigentes) en “invertir” la energía solar que reciben para formar enlaces químicos. Llegado el momento de aprovechar esa energía invertida, se rompen esos enlaces para formar otros, y la energía que sobra se utiliza para realizar otro trabajo (una nueva formación de enlaces o una alteración del estado de movimiento). Con algunas excepciones que son cosa de físicos, como la energía atómica, donde lo que se rompen no son enlaces químicos sino los núcleos de determinados átomos, el trajín de acumulación y transformación de energía en la Tierra es cosa de química. De la química de la energía.
Hay muchas sustancias diferentes que se usan como reservorios de energía y como agentes de transporte, aunque sorprendentemente están formadas por sólo unos pocos de los más de cien elementos químicos disponibles. Los “combustibles”, en concreto, están compuestos básicamente por carbono (C), hidrógeno (H) y oxígeno (O). Decíamos antes que para aprovechar la energía acumulada en los enlaces químicos teníamos que romperlos y formar otros. Una forma fácil de romperlos es combinar los átomos que une el enlace que queremos romper con oxígeno, elemento que abunda en la atmósfera y que siempre está ávido de electrones. El carbono, el hidrógeno y el oxígeno forman compuestos que reaccionan muy fácilmente con oxígeno, permitiendo aprovechar la energía que se desprende en la recombinación de enlaces. Así, la mayoría de las reacciones de extracción de energía son oxidaciones de compuestos formados por carbono, hidrógeno y oxígeno. Y esto abarca desde la reacción de combustión del motor de un coche, donde se consumen hidrocarburos (CxHy) y se libera calor, a la respiración celular de los seres vivos, donde se consumen glúcidos (CxHyOz) y se generan moléculas de ATP, la sustancia de intercambio energético en las células.
De cómo rompamos los enlaces químicos de nuestro combustible y formemos los de las sustancias derivadas dependerá el rendimiento energético que extraigamos. Vamos a poner un ejemplo con la reacción de combustión más sencilla, la del hidrógeno:
Cuando combinamos hidrógeno con oxígeno y les dejamos reaccionar libremente se combinan para formar agua. El oxígeno se entromete entre los electrones que comparten cada uno de los dos átomos que formaba la molécula de hidrógeno gas (H-H), rompiendo su enlace y formando dos nuevos (H-O-H). Como la energía que se gasta en romper el enlace H-H es menor que la que se libera al formar los H-O, sobra energía que se desprende en forma de calor. Podemos aprovechar ese calor para expandir un gas que empuje un mecanismo, transformando así energía química en energía mecánica. Es lo que ocurre en los motores de los vehículos o en los generadores eléctricos convencionales (aunque generalmente se usan otros combustibles, como el diésel o la gasolina, que son hidrocarburos). Este proceso, sin embargo, tiene un rendimiento limitado a la eficiencia del llamado ciclo de Carnot, donde se genera un trabajo aprovechando la diferencia de temperatura de dos partes de una máquina, expandiendo un gas isotérmicamente por aporte de calor, y comprimiéndolo también isotérmicamente retirando el calor sobrante. El rendimiento viene limitado en concreto por el cociente entre las dos temperaturas. La existencia de piezas móviles en un motor o generador disminuye además el rendimiento por rozamiento, haciendo que éste sea como máximo de un 35%.
Resulta mucho más eficiente mediar entre el hidrógeno y el oxígeno durante su reacción, capturando los electrones que el hidrógeno va a ceder al oxígeno y obligándoles, antes de llegar a él, a realizar el trabajo que queramos. De esta manera la reacción se divide en dos:
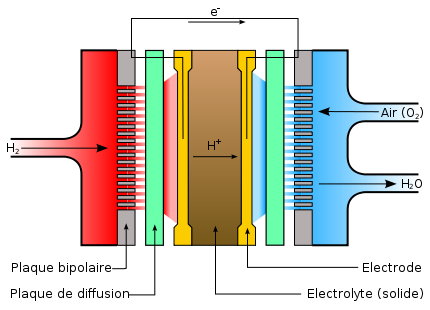
Para conseguir esto se separa el flujo de hidrógeno del de oxígeno por una membrana que solo pueden atravesar los protones (H+) y se colocan dos electrodos, uno a cada lado de la membrana (en amarillo en la imagen). Uno de ellos, el ánodo (izquierda), se encarga de recoger los electrones que suelta el hidrógeno (reacción superior). El otro, llamado cátodo (derecha), los cede al oxígeno, que combinado con los protones que han atravesado la membrana forma agua (reacción inferior). Entre el ánodo y el cátodo está el circuito que queramos alimentar con corriente eléctrica. Esta forma de transformar energía química en eléctrica tiene rendimientos mucho mayores a los de la estrategia anterior, de en torno al 70−80%. Para el caso de querer transformar energía química a mecánica podríamos utilizar un motor eléctrico, que presenta rendimientos mucho más altos que los térmicos, de en torno al 75%. Esta segunda estrategia es la que se emplea en las celdas de combustible, donde no se “quema” el combustible, sino que se somete a un proceso electroquímico, aprovechando la transformación directa de energía química en eléctrica, sin pasar por la térmica. Quemar combustibles fósiles para obtener energía vendría a ser como matar un cerdo para hacer solamente hamburguesas. Nos perdemos lo mejor.
Un último apunte. La naturaleza, que nos lleva eones de ventaja, tiene un mecanismo llamado “cadena de transporte de electrones” que aprovecha la energía química de los glucósidos de una manera similar a la empleada en las celdas de combustible. Menos mal, porque no me quiero imaginar lo incómodo que sería tener que quemar los macarrones en nuestro organismo en sentido literal…
PD. Gracias siempre a Clara por las sugerencias y correcciones.


 No hay comentarios
No hay comentarios